11 月 9 日,輝瑞(Pfizer, PFE-US)和BioNTech宣布了一個大消息:兩家聯合研發的新冠候選疫苗在III期臨床試驗中取得重大進展,在第二次注射後 7 天,疫苗有效率超過 90% 。

▲ 輝瑞 宣布新冠疫苗 有效率超過90%(來源:Pfizer)
如果這個疫苗安全性和有效性完全達標,他們計劃在 11 月的第三週,向美國食品藥品管理局(FDA)提交緊急使用授權。
聽到這個消息時,很多人都興奮了——參加試驗的志願者有 43,538 人,是不是說明這個疫苗比別的厲害多了?
但有的朋友可能注意到一個細節:“ 90% 有效率”,是根據“ 94 位感染新冠的受試者”的數據判斷的,這還只是第 1 次中期分析的結論。
如此短的時間內、得到這麼有限的數據,就能判斷疫苗的有效率嗎?
一、輝瑞新冠疫苗的試驗方案是什麼樣?
想必大家還記得,今年 9 月,阿斯利康由於一位受試者出現嚴重不良反應、曾暫停過新冠疫苗臨床試驗(回顧:突發,阿斯利康叫停新冠疫苗臨床試驗!專家:暫停不等於失敗)。
之後,各界都呼籲公開新冠疫苗試驗方案,提高資訊透明度——怕就怕病急亂投醫,萬一哪家的“問題疫苗”不明不白獲得了緊急使用許可,後果不堪設想。
沒錯,輝瑞也在風口(註:風口指投資機會或趨勢)浪尖之時,公佈了候選疫苗 BNT162b2 的I/II/III期試驗方案 ,你們今天聽說的這個III期試驗,就是它的一部分。
這項臨床試驗找的受試者,都是之前從沒感染過新冠的健康人,隨機雙盲分為 1 : 1 的兩組,分別接種候選新冠疫苗和安慰劑(“雙盲”就是,給受試者打疫苗的人和受試者本人,都不知道自己注射的是什麼,以免有心理作用影響實驗結果),然後正常生活(會要求注意避孕),定期隨訪。
延伸閱讀>> 財團法人醫藥品查驗中心:疫苗研發的臨床參考要點
二、III期試驗的主要結果是看什麼?
檢驗一個呼吸道病毒疫苗是否有效,不是看多少人打完疫苗沒感染,而是看接種候選疫苗的人裡,有多少人出現了感染病毒的症狀、而且測出了核酸陽性。
所以,這裡說的“疫苗有效率”,不是“完全預防感染新冠病毒”,而是“避免成為有症狀感染者”(所以不包括“預防無症狀感染”)。某些媒體直接說它“阻止了 90% 的感染”,措辭是不嚴謹的。
輝瑞這個試驗也是一樣,看的是受試者接種第 2 劑疫苗後一定時間內,有多少人出現了至少 1 種新冠感染症狀+鼻拭子核酸陽性。
美國FDA的標準是,新冠疫苗有效率最低要達到 50% ,才能獲得緊急使用許可。 (當然,這是及格線,正常情況下疫苗想要上市要求更高。)
輝瑞給自己定的小目標稍微高一些—— 60% 。
60% 的有效率是什麼概念呢?
假設打完安慰劑的人(也就是沒有疫苗保護)一年內的患病率是 1.3% ,那麼打了疫苗的人可以在此基礎上再減少 60% 的感染,也就是只有 0.52% 的患病率。
三、中期分析就能預測有效率,可靠嗎?
在這個過程中,每當有症狀的感染者達到一定數量,研究人員還會做一次中期分析(interim analysis)。
他們本來計劃做 4 次中期分析,後來和FDA討論後改成了 3 次。當有症狀感染者人數:
- 達到 62 人時,進行第 1 次中期分析
- 達到 92 人時,進行第 2 次中期分析
- 達到 120 人時,進行第 3 次中期分析
為什麼感染人數才這麼少就要分析一波呢?
其實,這是為了早點判斷疫苗的效果,看有沒有達到要求。分階段進行,每一小步都達標了,再判斷試驗要不要繼續下去。
但計劃總趕不上變化。等他們討論完後,發現真正收集到的感染人數已經有 94 例了……於是乾脆全部拿來進行第 1 次中期分析。
那麼 90% 的有效率,又是怎麼算出來的呢?
試驗計劃裡有一張表格,假設了每次中期分析的成功和無效標準,對應的疫苗有效率如下:
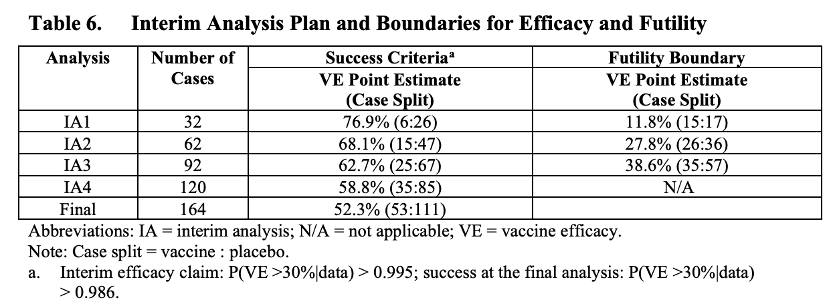
▲ IA=中期分析;VE=疫苗有效率。括號裡的比值就是疫苗組感染者:安慰劑組感染者的人數比值(來源:Pfizer)
譬如原計劃第 3 次中期分析是 92 人,假設疫苗組 25 人感染、安慰劑組 67 人感染(兩組人數相同),說明打疫苗降低了( 67-25 )/ 67 = 62.7% 的感染數,也就是保護效力為 62.7% 。
一旦達到了上面表格里有效率的成功點,就計劃向FDA提交緊急許可授權;沒達到就繼續試驗;而一旦低於了無效邊界,試驗就不用繼續了。
如果保護效力比這還高,疫苗組感染人數就會比 25 人更小。
所以,在僅有 94 人感染的情況下,就判斷有效率高達 90% ,並不是誇大其詞,而是有理有據算出來的。
既然疫苗效果如此超出預期,在這時申請緊急使用許可,給高危易感人群儘早用上、減少感染,也是合情合理。
不過,臨床試驗還沒結束之前,一切皆有可能。
中國目前進入 III 期臨床試驗的新冠疫苗有滅活疫苗和腺病毒載體疫苗。而輝瑞這款是mRNA疫苗,安全性和長期的保護效力究竟如何,還需要繼續監測。讓我們期待更多消息吧!
最後,給你幾個關鍵要點:
- 輝瑞新冠候選疫苗有效率高達 90% ,不是最終結論,而是第一次中期分析在受試者中收集到 94 例感染者得出的結果。
- 這裡的有效率不是“完全避免感染新冠病毒”,而是“避免成為有症狀感染者”,並不包括“避免成為無症狀感染者”。
- 疫苗可能藉此申請美國FDA的緊急使用許可,但臨床試驗還沒結束,疫苗的長期安全性和保護效果到底有多久,還需要繼續觀察。
參考文獻
- https://www.pfizer.com/news/press-release/press-release-detail/pfizer-and-biontech-announce-vaccine-candidate-against
- https://pfe-pfizercom- d8-prod . s3.amazonaws .com/ 2020-11 / C4591001_Clinical_Protocol_Nov2020 .pdf
本文作者:王鳳靈
審稿專家:盧學新(中國疾控中心病毒病預防控制研究所助理研究員、免疫學博士)
https://www.stockfeel.com.tw/輝瑞-新冠-疫苗-有效率/
